填補臨床空白��,為患兒家庭帶來(lái)治療新希望
全球特藥領(lǐng)域生物制藥公司益普生(Euronext:IPN;ADR:IPSEY)宣布其罕見(jiàn)病創(chuàng )新藥BYLVAY,Odevixibat capsules(中文:蓓爾唯�����,奧德昔巴特膠囊)在中國正式商業(yè)上市���,標志著(zhù)進(jìn)行性家族性肝內膽汁淤積癥(PFIC)領(lǐng)域治療藥物的可及性取得重大突破��。隨著(zhù)蓓爾唯的上市��,患者將有效提高生活質(zhì)量并長(cháng)期獲益����。此前���,奧德昔巴特已被納入3個(gè)省市惠民保國內特藥目錄及11個(gè)省市惠民保海外特藥目錄�,助力患者有藥可醫�、有藥可保���。
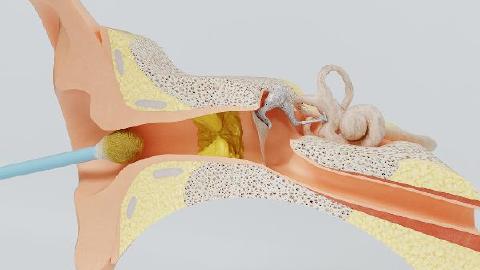
奧德昔巴特膠囊于2024年12月經(jīng)中國國家藥品監督管理局正式批準����,用于治療≥6月齡的PFIC患者的瘙癢�。PFIC是一種罕見(jiàn)的遺傳性疾病����,發(fā)病率為(1~2)/10萬(wàn)���,多在新生兒期或1歲以?xún)劝l(fā)病����,臨床表現包括黃疸��、瘙癢��、血清膽汁酸(SBA)值升高�、吸收不良和發(fā)育不良等�,常進(jìn)展為終末期肝病��,需要進(jìn)行肝移植[1]����。作為PFIC的一線(xiàn)治療藥物1����,奧德昔巴特是目前中國首個(gè)且唯一獲批治療PFIC領(lǐng)域的非手術(shù)靶向藥物����,為患者提供了有效安全的無(wú)創(chuàng )藥物治療選擇�����。
復旦大學(xué)附屬兒科醫院傳染感染科主任王建設教授表示:"PFIC是一類(lèi)進(jìn)展迅速的兒童罕見(jiàn)肝病����,可導致肝纖維化����、肝硬化和終末期肝臟并發(fā)癥��,常需要肝移植才能長(cháng)期存活��,部分亞型PFIC患兒僅有一半能自體肝存活至10歲[2]���。由于疾病罕見(jiàn)且臨床表現復雜���,疾病診療面臨諸多挑戰��。作為創(chuàng )新型回腸膽汁酸轉運體(IBAT)抑制劑藥物��,奧德昔巴特為PFIC患者提供了無(wú)創(chuàng )藥物治療新選擇�����,有助于降低血清膽汁酸�、改善瘙癢癥狀��,有望提高PFIC患兒自體肝長(cháng)期生存和生活質(zhì)量����。期待奧德昔巴特的上市能夠切實(shí)提高藥物可及性�����,為患兒及其家庭帶來(lái)更多獲益����。"
益普生中國總經(jīng)理Arkadiusz Budzinski表示:"作為一家深耕罕見(jiàn)病領(lǐng)域的特藥公司���,益普生始終以患者為中心����,致力于將罕見(jiàn)病創(chuàng )新藥物及療法加快引入中國�����。奧德昔巴特的上市是益普生在改善罕見(jiàn)病患者福祉���,提升藥物可及性方面取得的又一重要里程碑��。未來(lái)����,我們將持續攜手各方力量��,積極推動(dòng)奧德昔巴特惠及更多地區和患者�,助力構建罕見(jiàn)病診療與保障體系�����,照亮罕見(jiàn)病患者生命之光�。"
關(guān)于益普生
益普生是一家全球性的生物制藥公司�,專(zhuān)注于在腫瘤�����、罕見(jiàn)病和神經(jīng)科學(xué)三個(gè)治療領(lǐng)域為患者提供革新型藥物��。我們的研發(fā)管線(xiàn)由外部創(chuàng )新推動(dòng)�����,并由近100年的開(kāi)發(fā)經(jīng)驗以及位于美國��、法國和英國的全球中心提供支持���。我們的團隊遍布全球40多個(gè)國家��,在世界各地均有合作伙伴��,這使我們能夠為100多個(gè)國家的患者提供藥物���。
益普生在巴黎(泛歐交易所:IPN)上市并通過(guò)贊助的I級美國存托憑證項目(ADR:IPSEY)在美國上市交易�����。
關(guān)于益普生中國
益普生集團于1992年進(jìn)入中國��,于2021年在上海成立中國區總部�,并于2022年根據集團業(yè)務(wù)變動(dòng)�,同步剝離多元健康業(yè)務(wù)���,專(zhuān)注于特藥領(lǐng)域����,針對三大疾病領(lǐng)域(腫瘤����、罕見(jiàn)病�����、神經(jīng)科學(xué))���,益普生中國將持續推出創(chuàng )新治療方案以滿(mǎn)足中國患者亟待解決的治療需求��。
益普生-有關(guān)前瞻性聲明的警示說(shuō)明
本文件中包含的前瞻性聲明���、目標與預期��,基于益普生的管理戰略�����、當前觀(guān)點(diǎn)及假設����。這些聲明涉及已知和未知的風(fēng)險與不確定性����,可能導致實(shí)際結果�、績(jì)效或事件與本文件所述情況產(chǎn)生重大差異���。上述所有風(fēng)險因素均可能影響益普生未來(lái)達成財務(wù)目標的能力��,而這些目標是基于當前可獲取信息并假設宏觀(guān)經(jīng)濟環(huán)境相對穩定的前提下設定的�。本文件中使用的"相信""預計""期望"等詞語(yǔ)�,以及其他類(lèi)似表達�,旨在識別前瞻性聲明���,包括益普生對未來(lái)事項(如監管遞交與審批結果等)的預期���。此外��,本文件所述目標并未考慮外部增長(cháng)的假設或潛在的未來(lái)并購交易�����,這些因素可能導致相關(guān)指標發(fā)生變化���。這些目標基于益普生認為合理的數據和假設�,同時(shí)依賴(lài)于未來(lái)可能發(fā)生的情況��,而非完全依賴(lài)于歷史數據���。受若干風(fēng)險與不確定性影響���,實(shí)際結果可能與相關(guān)指標產(chǎn)生顯著(zhù)偏差��,例如某些在早期開(kāi)發(fā)或臨床階段具有前景的藥物���,最終可能因監管或市場(chǎng)競爭原因未能上市或未達成商業(yè)目標��。益普生需應對�,或可能需要應對仿制藥帶來(lái)的競爭����,這可能導致市場(chǎng)份額流失�。此外�,研發(fā)過(guò)程包含多個(gè)階段�,每一階段均存在益普生未能達成目標�、甚至被迫終止已投入大量資源的項目的重大風(fēng)險����。因此���,益普生無(wú)法保證在臨床前階段取得的積極結果一定能在后續臨床試驗中得到驗證�,也無(wú)法保證臨床試驗結果足以證明相關(guān)藥物的安全性與有效性���。產(chǎn)品是否能獲得監管批準����,或是否能在市場(chǎng)上取得商業(yè)成功����,也無(wú)法作出保證�����。若基本假設出現偏差����,或風(fēng)險與不確定性成為現實(shí)����,則實(shí)際結果可能與前瞻性聲明存在重大差異����。其他可能影響公司經(jīng)營(yíng)的風(fēng)險與不確定性還包括(但不限于):行業(yè)整體狀況與競爭格局���、宏觀(guān)經(jīng)濟因素(包括利率和匯率波動(dòng))�、醫藥監管政策與醫療立法影響�、全球控費趨勢�����、競爭對手的技術(shù)進(jìn)步與新藥/專(zhuān)利的取得���、創(chuàng )新藥物研發(fā)過(guò)程中固有的挑戰(包括獲取監管批準)���、益普生對未來(lái)市場(chǎng)的判斷能力���、生產(chǎn)延誤或困難���、國際金融不穩定性及主權風(fēng)險�、益普生對專(zhuān)利及創(chuàng )新藥物其他保護機制的依賴(lài)�、以及可能遭遇的訴訟(包括專(zhuān)利及合規訴訟)����。此外����,益普生在部分藥品的開(kāi)發(fā)和商業(yè)化中依賴(lài)第三方合作伙伴���,這些合作關(guān)系可能產(chǎn)生大額特許權收入�����。但相關(guān)方若行為不當�,可能對益普生的業(yè)務(wù)和財務(wù)結果造成不利影響��。益普生無(wú)法保證其合作伙伴將全面履約��,也可能無(wú)法從合作協(xié)議中獲得預期收益���。若合作方違約�,可能導致公司營(yíng)收低于預期���,對公司業(yè)務(wù)��、財務(wù)狀況或運營(yíng)表現造成負面影響�。除非適用法律另有要求����,益普生明確聲明無(wú)義務(wù)更新或修訂本新聞稿中的任何前瞻性聲明����、目標或預測�����,以反映相關(guān)假設或條件的變化��。益普生的業(yè)務(wù)亦受其向法國金融市場(chǎng)管理局提交的注冊文件中所述的風(fēng)險因素影響���。上述風(fēng)險與不確定性并非詳盡無(wú)遺���,建議讀者查閱益普生最新發(fā)布的通用注冊文件�����,可于官網(wǎng)獲取�����。
[1]McKiernan P,et al.JHEP Rep.2023;6(1):100949.
[2]JONES-HUGHES T,CAMPBELL J,CRATHORNE L.Epidemiology and burden of progressive familial intrahepatic cholestasis:A system?atic review[J].Orphanet J Rare Dis,2021,16(1):255.DOI:10.1186/s13023-021-01884-4.